Allgemeine Vorbemerkungen
Der Bildungsplan zeichnet sich durch Inhalts- und Kompetenzorientierung aus. In jeder Bildungsplaneinheit (BPE) werden in kursiver Schrift die übergeordneten Ziele beschrieben, die durch Zielformulierungen sowie Inhalts- und Hinweisspalte konkretisiert werden. In den Zielformulierungen werden die jeweiligen fachspezifischen Operatoren als Verben verwendet. Operatoren sind handlungsinitiierende Verben, die signalisieren, welche Tätigkeiten beim Bearbeiten von Aufgaben erwartet werden. Die für das jeweilige Fach relevanten Operatoren sowie deren fachspezifische Bedeutung sind jedem Bildungsplan im Anhang beigefügt. Durch die kompetenzorientierte Zielformulierung mittels dieser Operatoren wird das Anforderungsniveau bezüglich der Inhalte und der zu erwerbenden Kompetenzen definiert. Die formulierten Ziele und Inhalte sind verbindlich und damit prüfungsrelevant. Sie stellen die Regelanforderungen im jeweiligen Fach dar. Die Inhalte der Hinweisspalte sind unverbindliche Ergänzungen zur Inhaltsspalte und umfassen Beispiele, didaktische Hinweise und Querverweise auf andere Fächer bzw. BPE.
Der VIP-Bereich im Bildungsplan umfasst Vertiefung, individualisiertes Lernen sowie Projektunterricht. Im Rahmen der hier zur Verfügung stehenden Stunden sollen die Schülerinnen und Schüler bestmöglich unterstützt und bei der Weiterentwicklung ihrer personalen und fachlichen Kompetenzen gefördert werden. Die Fachlehrerinnen und Fachlehrer nutzen diese Unterrichtszeit nach eigenen Schwerpunktsetzungen auf Basis der fächerspezifischen Besonderheiten und nach den Lernvoraussetzungen der einzelnen Schülerinnen und Schüler.
Der Teil „Zeit für Leistungsfeststellung“ des Bildungsplans berücksichtigt die Zeit, die zur Vorbereitung, Durchführung und Nachbereitung von Leistungsfeststellungen zur Verfügung steht. Dies kann auch die notwendige Zeit für die gleichwertige Feststellung von Schülerleistungen (GFS), Nachbesprechung zu Leistungsfeststellungen sowie Feedback-Gespräche umfassen.
Fachbezogene Vorbemerkungen
„Dass ich erkenne, was die Welt im Innersten zusammenhält“ (Goethe, Faust I). Die Beantwortung dieser Frage ist sowohl für den einzelnen Menschen als auch für die Gesellschaft außerordentlich wichtig. Als Naturwissenschaft liefert die Chemie dazu einen wesentlichen Beitrag. Ziel eines zeitgemäßen Chemieunterrichtes ist deshalb, jeden Einzelnen zu befähigen, seiner Verantwortung in allen Bereichen der Technik, Wirtschaft, Ökologie und Kultur bewusst nachzukommen.
Fachliche Aussagen zum Kompetenzerwerb in der Mittelstufe
Naturwissenschaftliche Kompetenz zeigt sich darin, die charakteristischen Eigenschaften unserer Umwelt sowie die Bedeutung der Naturwissenschaften in unserer heutigen Welt zu verstehen. Sie befähigt die Lernenden, naturwissenschaftliches Wissen anzuwenden, um Fragestellungen zu erkennen, naturwissenschaftliche Phänomene zu beschreiben und aus Belegen Schlussfolgerungen zu ziehen. Diese Kompetenz schließt auch die Bereitschaft mit ein, sich reflektierend mit naturwissenschaftlichen Ideen und Themen auseinanderzusetzen und ermöglicht es den Schülerinnen und Schülern darüber hinaus Problemstellungen zu bewältigen, die wir heute noch nicht kennen.
Der Bildungsplan für den Chemieunterricht zielt deshalb auf das Verständnis und die Anwendung grundlegender chemischer Begriffe, Gesetzmäßigkeiten, Konzepte und Modelle ab. Gelungene naturwissenschaftliche Bildung zeigt sich in der Fähigkeit, chemische Fragestellungen zu erkennen, chemisches Wissen anzuwenden, aus chemischen Fakten Schlussfolgerungen zu ziehen und Bewertungen aufgrund einer naturwissenschaftlich-rationalen Abwägung vorzunehmen. Dazu sind sowohl inhaltsbezogene als auch prozessbezogene Kompetenzen nötig.
Der Bildungsplan legt das Anforderungsniveau gemäß der Bildungsstandards für den Mittleren Schulabschluss der Kultusministerkonferenz in diesem Fach zu Grunde. Die Bildungsstandards definieren bezüglich der chemischen Fachkompetenz vier Fachkompetenzbereiche, die – wie auch in den anderen Naturwissenschaften – eine Inhaltsdimension und eine Handlungsdimension umfassen. Die Inhaltsdimension wird überwiegend im Kompetenzbereich Fachwissen, die Handlungsdimension in den Kompetenzbereichen Erkenntnisgewinnung, Kommunikation und Bewertung dargestellt. Inhalts- und handlungsbezogene Kompetenzen greifen ineinander und werden in der Regel gemeinsam erworben. Durch das Zusammenwirken der vier Fachkompetenzbereiche entwickelt sich die chemische Fachkompetenz.
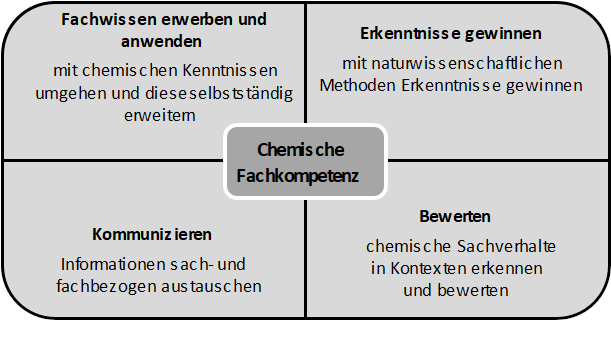
- Fachwissen: Die chemischen Fachinhalte (wie z. B. chemische Phänomene, grundlegende Begriffe und Gesetzmäßigkeiten, Prinzipien der Chemie) können in der Sekundarstufe I auf vier Basiskonzepte (Stoff-Teilchen-Beziehungen, Struktur-Eigenschafts-Beziehungen, chemische Reaktion und energetische Betrachtung bei Stoffumwandlungen) zurückgeführt und mit deren Hilfe strukturiert und sowohl horizontal wie vertikal vernetzt werden.
- Erkenntnisgewinnung: Die Denk- und Arbeitsweise in der Chemie findet in diesem Fachkompetenzbereich ihren Niederschlag: Durch Experimente oder mithilfe geeigneter Modellvorstellungen werden Kompetenzen neu erworben oder vorhandene weiterentwickelt.
Die Verknüpfung gewonnener Erkenntnisse mit bereits geläufigen Konzepten, Modellen und Theorien führt zur Fähigkeit, chemische Phänomene zu erkennen und zu erklären. - Kommunikation: Für einen fachbezogenen reflektierenden Informationsaustausch gilt es eine Kommunikationskompetenz zu entwickeln, in der eine sachgemäße Verknüpfung von Alltags- und Fachsprache gelingt. Neben der verbalen Form des Kommunizierens lassen sich chemische Zusammenhänge je nach Kontext und Inhalt auch in anderen Formen wie der symbolischen und mathematischen Form darstellen.
- Bewertung: Durch eine gezielte Auswahl chemierelevanter Kontexte gelingt es den Schülerinnen und Schülern, die Vernetzungen der Chemie in Lebenswelt, Alltag, Umwelt und Wissenschaft zu erkennen, zu reflektieren, zu bewerten, sachgerecht ihre eigene Meinung zu vertreten und ihr Handeln anzupassen.
Zu beachten ist, dass die Vermittlung sowohl der inhaltsbezogenen wie auch der prozessbezogenen Kompetenzen gezielt in der Unterrichtsplanung und in den Lernzielkontrollen zu berücksichtigen ist. Damit wird es zu einem wichtigen Ziel des Chemieunterrichts, die Schülerinnen und Schüler zum selbstständigen Anwenden chemischer Denk- und Arbeitsweisen zu führen und explizit eine möglichst weitgehende Durchdringung von naturwissenschaftlichen Zusammenhängen zu ermöglichen.
Weitere Hinweise
Diese vier Kompetenzen werden in einem Chemieunterricht entwickelt, der seinen Beitrag dazu leistet,
- bei den Schülerinnen und Schülern Interesse zu wecken und sie zu motivieren, sich mit chemischen Fragestellungen auseinander zu setzen,
- lebensweltbezogene Aspekte einzubeziehen, z. B. durch die Auswahl von „Lerngegenständen“, die für die Schülerinnen und Schülern jetzt und im späteren Leben relevant sind (siehe Gemeinsamer Referenzrahmen für Naturwissenschaften (GeRRN), MNU Oktober 2017),
- durch Demonstrations- und Schülerexperimente in exemplarischer Weise den empirischen Charakter der Naturwissenschaft Chemie zu verdeutlichen,
- das Denken in Modellen und die Modellbildung zu schulen,
- eine korrekte Fachsprache zu nutzen und einzufordern,
- Basiskonzepte (Stoff-Teilchen, Struktur-Eigenschaften, chemische Reaktion, energetische Betrachtungen bei Stoffumwandlungen) zu vermitteln,
- Schülerinnen und Schüler zu einem sicheren, zeitgemäßen und nachhaltigen Umgang mit Ressourcen (Stoffen und Energie) zu erziehen (im Sinne einer Bildung für nachhaltige Entwicklung),
- naturwissenschaftliche Fragestellungen in fächerübergreifenden Kontexten zu betrachten und zu bewerten,
- einen Ausblick auf globale Zusammenhänge zu geben.
Durch die bewusste Entwicklung der genannten Kompetenzen und durch anschlussfähiges, berufsbezogenes Lernen werden die Schülerinnen und Schüler befähigt, die breitgefächerten Angebote des Bildungssystems nach ihren individuellen Interessen und Begabungen wahrzunehmen. Darüber hinaus eröffnet der Chemieunterricht zusammen mit den anderen Naturwissenschaften Perspektiven für den weiteren Bildungsweg und die spätere Berufs- und Studienwahl, insbesondere in chemisch-technischen und weiteren naturwissenschaftlichen Berufsfeldern.
